抗疫新药启动三期临床试验,医药投资人:动作很快,有戏
编者按:本文来自微信公众号“投资界”(ID:pedaily2012),作者任倩,36氪经授权发布。
 在疫情阴霾下,大家热切期待真正的靠谱药面世。
在疫情阴霾下,大家热切期待真正的靠谱药面世。2月1日,美国吉利德公司发布声明,称公司正与全球卫生机构密切合作,提供在研药物Remdesivir(瑞德西韦)用于新型冠状病毒试验性治疗。昨日,吉利德与中国医学科学院药物研究所联合申报瑞德西韦,获得国家药品监督管理局受理。
这是一款被视为治疗新型冠状病毒的“特效药”。1月31日,权威医学期刊《新英格兰医学杂志》发表多篇关于新型冠状病毒病例的论文,其中一篇提到:病人于住院第7天晚上开始使用药物Remdesivir,次日退烧(体温从前一天的39.4摄氏度降低到次日的37.3摄氏度),症状明显减轻。
值得注意的是,这种药物并非为新冠病毒专门开发的新药,它是吉利德针对埃博拉病毒开发的一款药物,目前该药在中国并未上市。
上海市公共卫生临床中心党委书记、卫健委专家组卢洪洲教授在接受解放日报·上观新闻采访时表示,目前卫健委专家组已写好方案及申请,并汇报上级部门,直接联系吉利德公司,并申请Remdesivir绿色通道。另外,中国临床试验注册中心网站消息显示,该研究将于2月3日在中日友好医院正式启动。新药开发通常是完成三期临床试验后提交上市注册申请。
消息一出,一位长期从事医药行业的知名投资人对投资界兴奋地说道:“这次动作很快!感觉有戏。等临床试验结果吧,三期临床是研发上市前最后一个环节,如果有疗效,药监局会加快审批,整个过程应该会很短。”
特效药还要等多久?动作快,抗疫新药今天启动三期临床
新型冠状病毒感染人数不断攀升,当下是否已有针对性的有效药物和疫苗?研发进度如何?这是我们每个人都万分关注的问题。疫情蔓延下,全球医疗界的目光都投向了中国,携手研发药物、疫苗,共同对抗病毒的动作也越来越快。
除吉利德外,包括艾伯维、强生等在内的国际知名抗病毒药企也都表示愿意与中国卫生监管机构密切合作,而国内企业海正药业也因法匹拉韦的研发也受到关注。
根据医药魔方NextPharma收录的信息,当前在研的抗2019-nCoV病毒感染项目已经有7个,除了最近为众人所知的阿比多尔、瑞德西韦(吉利德,RNA聚合酶抑制剂)、法匹拉韦(海正药业,RNA聚合酶抑制剂)、洛匹那韦(艾伯维,蛋白酶抑制剂)等小分子抗病毒药物外,还有诸如CR3022等针对S蛋白的大分子单抗药物,只不过还处于临床前研究阶段。
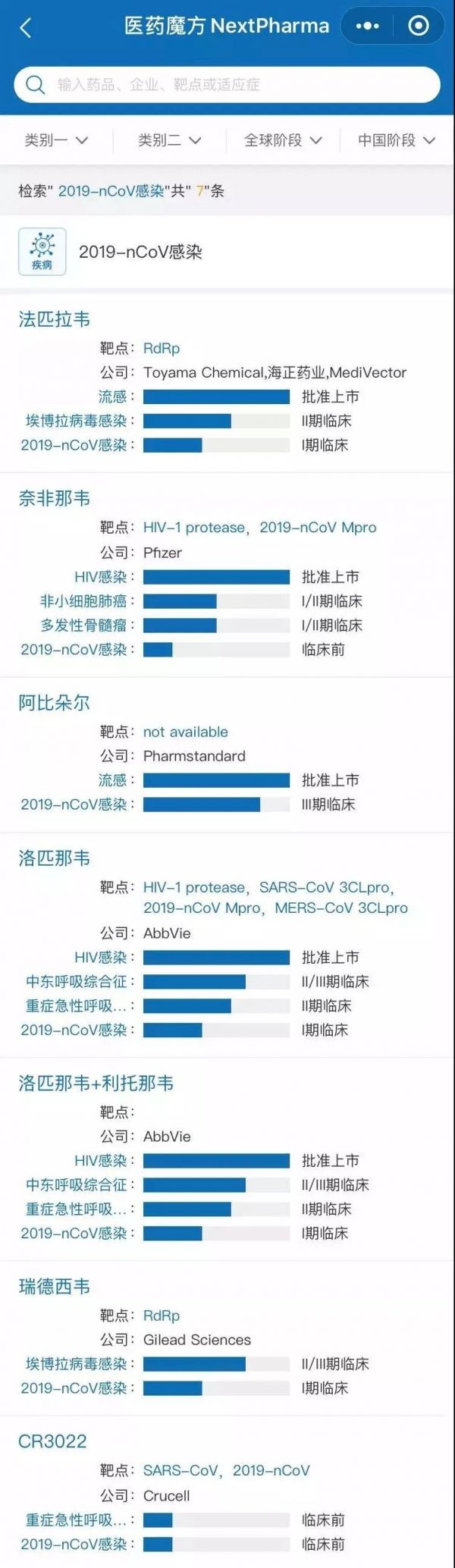
兵贵神速。那这些药到底有没有用?针对大量患者的药物仍需要经过临床试验来验证。而目前,这些企业都已在临床阶段紧锣密鼓地推进中。
以“新型冠状病毒”为关键词在中国临床试验注册中心(www.chictr.org.cn)中检索发现,目前已经登记启动了7项研究,在武汉、广州、重庆、北京等4地开展,试验药物涉及中药、血必净注射液、糖皮质激素、利巴韦林+干扰素α-1b、洛匹那韦/利托那韦+干扰素-α2b等。
而以“2019-nCoV”为关键词在医药魔方PharmaGo全球临床试验库中检索发现,目前已经登记启动了3项研究,其中有2项是治疗性研究。一项是来自中南大学湘雅医院开展的阿比多尔治疗研究,一项是北京协和医院发起的甲泼尼龙的治疗研究。
其中,最受关注的则是吉利德公司研发的抗病毒药Remdesivir(瑞德西韦),这是一种此前计划用于埃博拉病毒治疗的核苷酸类似物前药,但也被认为可能对冠状病毒可以起到抑制作用。
据了解,该项三期临床试验计划将于2020年2月3日在中日友好医院正式启动,可谓火速进行。此次三期临床试验将由首都医科大学作为申办方,计划入组270名相关患者,而牵头研究者为中日医院呼吸与危重症医学科主任兼呼吸与危重症医学科二部(含临床微生物与感染实验室、结核病区)主任曹彬教授。
在此之前,抗HIV病毒药品克力芝被视为抗击新型冠状病毒首个脱颖而出的关键药品。克力芝本是一种抗艾滋病的药物,广为人知是因北京大学第一医院呼吸和危重症医学科主任、国家卫健委专家组成员王广发接受采访时表示,克力芝对其个例来说是有效的。1月26日,官方证实克力芝的确对新型肺炎有效。
除了已经启动临床研究的跨国药企和国内本土大药企外,部分创新药企业也在加急研发中。比如德益阳光核心团队自2002年就开始在美国从事抗病毒创新药的研发,2013年公司成立之初第一个产品就选择针对被忽视的、新型的病毒创新药。
其首发适应症本来选择移植后的慢性诺如病毒感染,预防性和治疗性药物已经通过FDA的Pre-IND Meeting,2月份提交美国临床试验。在武汉疫情爆发后加急研发扩展适应症,从作用机理和SARS、冠状病毒等细胞/动物模型上验证可能对新型冠状病毒有效。
不过,要想大规模推广应用,这些药物都要靠实实在在的临床试验结果说话。
疫苗还要等多久?集全球之力,疫苗也正在路上
在国内外加紧药物研发的同时,疫苗也在赶来的路上。
1月28日,国家卫健委高级别专家组成员、中国工程院院士李兰娟在接受采访时表示,已经成功分离出了3株新型冠状病毒的毒株,这意味着已经拥有了疫苗的种子株。
同一天,香港大学医学院微生物学系传染病学讲座教授、国家卫健委高级别专家组成员袁国勇表示,港大微生物学系初步在喷鼻式流感疫苗基础上,已研发出针对新型冠状病毒的疫苗,未来可进行动物实验,明确疫苗的有效性和安全性,疫苗有望于1年内对人体展开临床测试。
与此同时,同济大学附属东方医院与斯微(上海)生物联手的新型冠状病毒mRNA疫苗研发正式立项。研发团队将在40天内完成大规模预防性疫苗样品的生产和制备,疫苗样品制作完成后,可以送国家指定机构开展抗新型冠状病毒活性测试,完成必要的审批后,可尽快推向临床。
实际上,本次疫情是CEPI(国际防范流行病创新联盟)在MERS之后应对的最大规模疫情,目前WHO也正在从国际层面协调全球的新型冠状病毒疫苗研发工作,CEPI正在与WHO进行紧急磋商。
1月30日,Inovio Pharmaceuticals公司宣布,将与艾棣维欣(Advaccine)携手加快在中国开发Inovio旗下对新型冠状病毒(2019-nCoV)的疫苗——INO-4800。Inovio计划尽快开发INO-4800疫苗,目前已经开始临床前测试和准备,以便为临床产品生产做准备。流行病防范创新联盟(CEPI)已经向Inovio提供高达900万美元的资助,以支持INO-4800在美国通过1期人体试验,评估疫苗的安全性和免疫原性。
艾棣维欣生物制药位于苏州工业园区,公司通过其特有的疫苗佐剂筛选与评价技术平台,已经研发出多款预防性及治疗性疫苗候选产品,覆盖呼吸道合胞病毒(RSV)肺炎疫苗、乙型肝炎病毒(HBV)疫苗等传染病领域。
1月30日,前沿生物与中国科学院上海药物研究所宣布针对抗2019-nCoV新药开发达成项目合作。上海药物所蒋华良院士和柳红教授领衔的团队研制的候选新药DC系列在抑制2019-nCov病毒以及其中关键蛋白试验中显示了较强的活性。
1月28日,三叶草生物制药宣布正式启动武汉新型冠状病毒(2019-nCoV)疫苗的研发。2019-nCoV是RNA病毒,其表面抗原S蛋白也具有天然三聚体结构,病毒通过其三聚体抗原(S蛋白)与宿主细胞表面ACE2受体结合,从而进入人体细胞,导致发烧、肺部感染等疾病。
与此同时,1月29日,药明生物宣布,公司紧急推动多个通过国际合作引进的2019新型冠状病毒(2019-nCoV)中和抗体开发。初步研究表明这些来自全球生物技术公司的抗体可有效中和新型冠状病毒。
投资团队建议:当下最急需加强抗病毒领域研究
多家医药企业加急研发新药,体现了中国创新能力及速度,但短时间研发成功并非易事。
中国医药创新促进会执行会长宋瑞霖曾建议,无论是资本,还是科学家、制药企业,要认识到医药和医疗是一个整体。有医无药,医从何来;有药无医,药给谁用,它们俩从来是一个整体。他呼吁,当下,必须要做市场最急需的。
清科医疗团队在做了大量研究工作后分析,2003年非典事件曾有过深刻教训,但那时中国的药物研发能力还不足。2010年后随着大批海归科学家回国创业以及创新药投资领域资金的加持,国内新药研发能力得到快速提升,更是具备了做国产新药的能力。
2019年NMPA共批准了58款创新药(包括化药1类和5.1类,生物制品1类和2类、中药和疫苗)上市,涵盖癌症、罕见病、抗病毒感染如丙肝、流感,免疫类、神经系统、泌尿系统、皮肤病等多个治疗领域。其中,抗癌药最多,共计12款抗癌药物首次获得批准上市,占比20.34%。
2018年,我国创新药临床申请主要集中在抗肿瘤领域,在整个创新药领域占比大约50%,且同靶点扎堆情况严重,尤其体现在以PD-1/L1和CAR-T为代表的靶点或技术领域;而抗病毒占比仅仅不到20%,并且多以乙肝、丙肝等大病为主。
相对于过度火热的肿瘤领域,抗病毒药物研发,尤其是被忽视的、新型的病毒研发显得微不足道。
可能抗病毒药物覆盖更多的人群,更广泛的群体,在商业层面上不如肿瘤来的更精准;也可能未来上市后经济价值回报相对小,但是谁都不做,何来治疗?
因此,他们呼吁,“加强抗病毒领域研究(尤其是被忽视的、新型的病毒),从企业、到投资、到政府资金加强投入与支持,而不要扎堆肿瘤。”
从院所、高校基础科研投入,比如细胞模型建立、动物药效、药代动力学、毒理等基础研究;到投资机构助力创新型企业进行原始创新、成果转化、产业化;到国家战略层面扶持、采购、储备;形成体系化的产业生态。
这是一场与死神赛跑的研发行动。中国有能力做自己的新药,有能力应对突发的疫情,靠谱的药物研发速度也不会甘于落后。
相关推荐
抗疫新药启动三期临床试验,医药投资人:动作很快,有戏
推进一类新药临床研究,「同源康医药」完成2.6亿元B轮融资
研发双抗创新药,「爱思迈生物」获得数千万元A+轮融资
成立3年敲钟挂牌香港联交所,肿瘤创新药研发商「德琪医药」加速推进核心产品市场化
36氪首发 | 医药临床试验的SaaS,「铨融医药科技」获得数千万元A+轮融资
「亚虹医药」获数亿元C轮融资,加快推进全球首创新药研发
“不创新是等死,创新可能会早死”,焦虑的药企老总们扎堆创新药
加快推进乙肝创新药临床,「挚盟医药」完成2.3亿元A轮融资
高瓴百亿重仓的“卖铲子”行业,干的是医药界富士康的生意?
中国抗体本周启动招股,云南白药已斥资3.5亿元成其基石投资者
网址: 抗疫新药启动三期临床试验,医药投资人:动作很快,有戏 http://www.xishuta.com/newsview16987.html
推荐科技快讯

- 1问界商标转让释放信号:赛力斯 95792
- 2报告:抖音海外版下载量突破1 25736
- 3人类唯一的出路:变成人工智能 25175
- 4人类唯一的出路: 变成人工智 24611
- 5移动办公如何高效?谷歌研究了 24309
- 6华为 nova14深度评测: 13155
- 7滴滴出行被投诉价格操纵,网约 11888
- 82023年起,银行存取款迎来 10774
- 9五一来了,大数据杀熟又想来, 9794
- 10手机中存在一个监听开关,你关 9519